Про те, як і навіщо гинуть живі клітини, в ефірі науково-популярної програми «Всесвіт» радіостанції «Голос Києва» розповів молодший науковий співробітник лабораторії нанобіотехнологій відділу молекулярної імунології Інституту біохімії імені О.В. Палладіна НАН України Кирило Пиршев.
Запрограмована клітинна загибель (апоптоз, загибель без запалення) є надзвичайно важливим для будь-якого живого організму процесом. Він зумовлений необхідністю регулярної заміни пошкоджених клітин, нездатних повноцінно виконувати свої функції, новими – задля забезпечення стабільності функціонування всього організму.
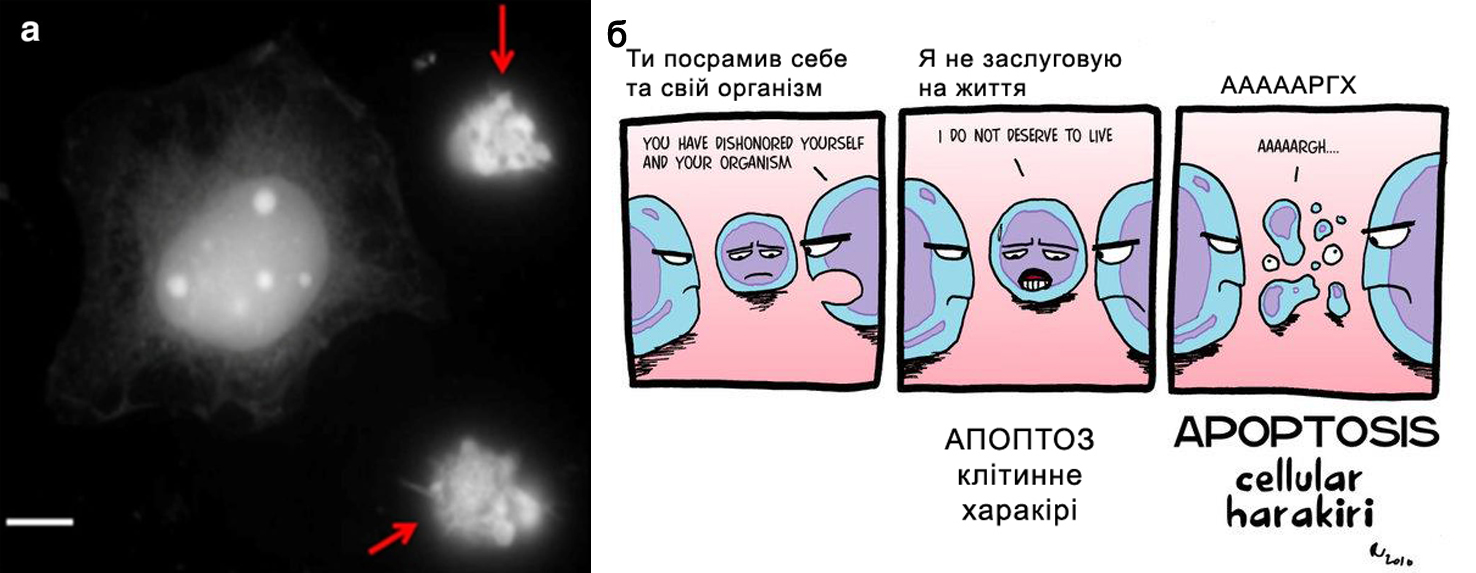 На зображеннях:а) мікрофотографія апоптозу в епітеліальних клітинах лінії HeLa, забарвлених карбоновими наночасточками (стрілками показано клітини, що вмирають; шкала розміру 10 мкм); б) апоптоз – «клітинне харакірі» (автор ілюстрації – Pedro Velica; original: https://velica.deviantart.com/art/Harakiri-176674972)
|
В живих клітинах апоптоз контролюється багатьма різними органелами й відбувається в кілька етапів. Рушієм слугує певний чинник впливу – внутрішній (коли в клітині накопичується критична кількість уражень) або зовнішній (коли клітина отримує від імунної системи сигнал про свою непотрібність: це відбувається, наприклад, під час ембріогенезу людини, коли плід позбувається шкірних перетинок між пальцями кінцівок).
Наступний етап – «прийняття рішення», після якого можливі два варіанти розвитку подій: клітина програмує себе або на вмирання, або на відновлення. Якщо започатковується процес самознищення, то клітина починає синтезувати відповідні протеїни (білки), котрі поступово руйнують її внутрішнє середовище. Внаслідок цього вона, врешті-решт, розпадається на бульбашкоподібні шматочки – везикули, – що в подальшому слугують джерелом живлення для сусідніх клітин. У разі некрозу (загибель із запальним процесом) відбувається пошкодження клітинної мембрани (клітинної «оболонки») із вивільненням усіх органел і ферментів у навколишнє середовище – міжклітинний простір. Таким чином, некроз однієї клітини становить небезпеку для інших клітин і може призводити до їхньої загибелі як на невеликих ділянках, так і на цілих ареалах. Якщо ж на етапі «прийняття рішень» обирається інший варіант – продовження життєдіяльності, – то клітина розпочинає процес аутофагії (самопоїдання): з цією метою вона формує аутофагосому (що надалі поєднується із лізосомою) – клітинний шлуночок, який огортає та перетравлює уражену частину клітини. «Тобто клітина сама себе й полікувала, й підживила», – пояснює К. Пиршев.
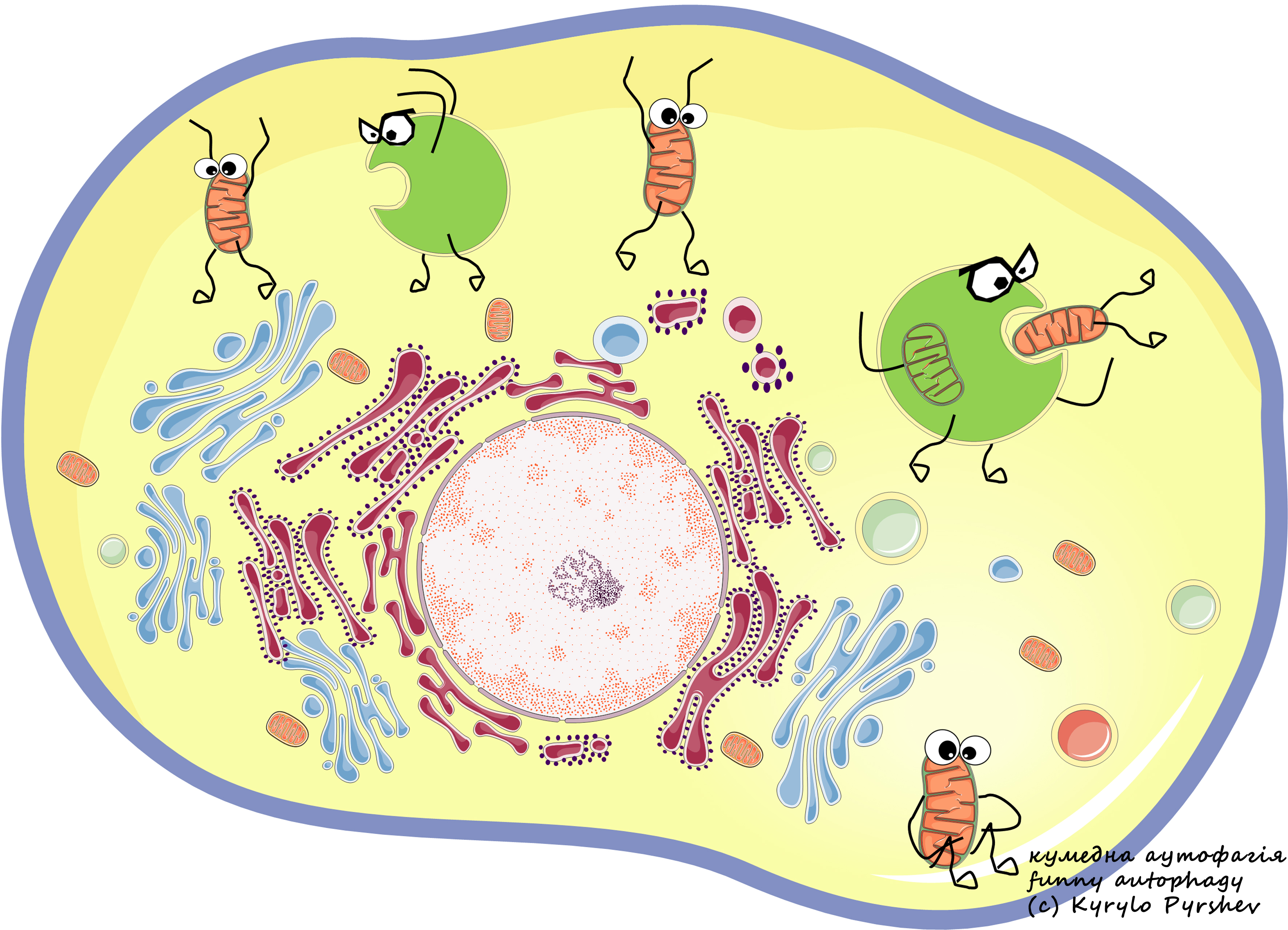 Жартівлива ілюстрація процесу аутофагії: лізосоми бігають за органелами (мітохондріями). Автор – Кирило Пиршев. Для підготовки зображення використовувалися зразки блок-схем, представлені на сайті Servier Medical Art |
Від належного перебігу процесів загибелі чи відновлення клітини залежить стан організму в цілому, адже в разі їхнього порушення можуть відбуватися небезпечні для життя та здоров’я патологічні зміни. Якщо під час апоптозу клітина з тих чи інших причин не може померти сама – вона починає неконтрольовано ділитися і створює підґрунтя для виникнення онкологічного захворювання. Неправильне оновлення так само може обернутися для організму онкогенезом, а ще – нейродегенеративними й автоімунними захворюваннями, дерматитами тощо.
Попри те, що наукові дослідження процесів апоптозу й аутофагії безперечно належать до фундаментальних (до речі, здобутки, отримані за цими напрямами, відзначено двома нобелівськими преміями в галузі фізіології та медицини – 2002 і 2016 років відповідно), вони можуть мати значну практичну користь у майбутньому – при створенні ефективніших медичних препаратів для лікування патологій, пов’язаних із цими біологічними процесами.
За словами К. Пиршева, нині вчені різних країн працюють над тим, щоб навчитися цілеспрямовано змінювати поведінку клітини – прискорювати її відмирання або подовжувати оновлення. Однак для досягнення потрібного результату, придатного для застосування не лише in vitro, а й in vivo, знадобляться десятки років.
Дослідження процесу клітинної загибелі, як зазначив гість радіопередачі, зараз мають переважно інтегративний характер і дедалі частіше здійснюються на межі кількох галузей науки – біохімії, молекулярної біології, фізіології, біофізики. Це дає змогу вивчати об’єкт комплексно, охоплюючи максимальну кількість пов’язаних із ним проблем.
 К. Пиршев здійснює контроль щільності популяції клітин під час роботи в культуральній (Київ, Україна) |
 К. Пиршев спостерігає в мікроскоп за інфузорією-туфелькою (Музей здоров’я, Г’юстон, США) |
ПРОСЛУХАТИ АУДІОЗАПИС РАДІОПЕРЕДАЧІ